Biokimistët kanë përdorur mikroskopi krio-elektron për të përcaktuar arkitekturën e detajuar të kanalit klorid TMEM16A. Kjo proteinë është një objektiv premtues për zhvillimin e barnave efektive për trajtimin e fibrozës cistike.
Fibroza cistike është një sëmundje e trashëgueshme e mushkërive, për të cilën aktualisht nuk ka shërim. Shkaku themelor i sëmundjes është mosfunksionimi i CFTR i kanalit klorid, i cili parandalon sekretimin e klorurit në disa qeliza të trupit. Kjo çon në dehidratimin e shtresës mukoze në mushkëri, shkruan Science Dialy transmeton Gazeta Shneta.
Një qasje premtuese për trajtimin e fibrozës cistike është aktivizimi i kanalit klorid të aktivizuar me kalcium, TMEM16A, si një rrugë alternative për rrjedhjen e klorurit. Meqenëse TMEM16A shprehet në epitelin e njëjtë si CFTR, aktivizimi i tij mund të rivendosë hidratimin e shtresës mukoze.
TMEM16A është pjesë e një familje proteine, anëtarët e së cilës lehtësojnë rrjedhën e joneve të kloridit të ngarkuar negativisht ose lipideve nëpër membranën qelizore. Struktura e një kanali klorur përcaktohet si Struktura e një shamblase TMEM16, e cila funksionon si një transportues i lipideve dhe luan një rol të rëndësishëm në koagulimin e gjakut, tashmë ishte i njohur nga puna e mëparshme.
Studiuesit e Departamentit të Biokimisë në Universitetin e Cyrihut tani kanë arritur gjithashtu në dekriptimin e strukturës së kanalit të kloridit TMEM16A. Për ta bërë këtë, ekipi i udhëhequr nga Profesor Raimund Dutzler përdori mikroskopin krioelektronik (cryo-EM), një teknikë, pionierët e të cilëve kohët e fundit morën çmimin Nobel në Kimi. “Arkitektura molekulare e kësaj proteze të membranës është vendimtare për zhvillimin e shënjestruar të barnave për trajtimin e fibrozës ciste”, thekson Dutzler.
Zbulimi i një mekanizmi të riaktivizimit të romanit
Kanali klorid TMEM16A mund të gjendet në organe të ndryshme të trupit dhe luan një rol kyç në sekretimin e klorurit në mushkëri, tkurrjen e muskujve të lëmuar dhe perceptimin e dhimbjes. Si ndryshon struktura e saj nga skramblazat e lidhur ngushtë me të njëjtën familje dhe se si proteina është aktivizuar nga kalciumi u zbulua tani nëpërmjet një kombinimi të krio-EM dhe elektrofiziologjisë.
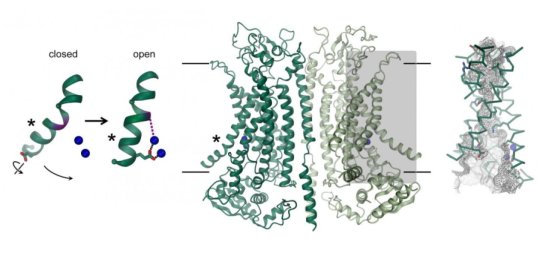
Ndërsa arkitektura e saj e përgjithshme i ngjan shamblazave të së njëjtës familje, ka dallime të dallueshme në rajonin e poreve që ndodhet në secilën nën-njësi të proteinës dimerike. Shamblazhat përmbajnë një brazdë polare të ekspozuar ndaj membranës, e cila lejon përhapjen e grupeve të kokrrizave lipide nëpër dyfishin lipid. Në të kundërt, në të njëjtin vend, TMEM16A formon një kanal të mbyllur me proteina në orë, i cili mbyllet në mungesë të kalciumit.
Lidhja e joneve të kalciumit të ngarkuar pozitivisht në afërsi të saj hap kanalin dhe lejon që jonet e klorureve të ngarkuara negativisht të përshkojnë nëpër membranën. “Ky mekanizëm i aktivizimit është unik, pasi që jonet e kalciumit të lidhur ndryshojnë drejtpërdrejt strukturën dhe elektrostatinë e poreve të depërtimit jon”, shpjegon Cristina Paulino, autore kryesore e studimit.
Duke hapur rrugën për terapi të reja Gjetjet që përshkruajnë strukturën dhe funksionimin e TMEM16A hapin rrugën për një kuptim mekanik të kësaj familjeje të rëndësishme të proteinave të membranës dhe japin një model premtues për zhvillimin e barnave për trajtimin e fibrozës cistike. “Substancat që çojnë në aktivizimin e TMEM16A do të kompensonin defektin në sekretimin e joneve të klorureve në mushkëri,” thotë Raimund Dutzler. / Gazeta Shneta